
原标题:双酰胺类杀虫剂作用机制及其先导优化研究进展
双酰胺类杀虫剂是一类以芳香环为核心,在芳香环的2个不同位点分别连接一个酰胺键的活性分子。第一个登记(2007年)的代表品种是日本农药株式会社研发的氟苯虫酰胺(亦称氟虫双酰胺,英文名flubendiamide,实验代号nni-0001)。此类杀虫剂作用靶标新颖,为昆虫鱼尼丁受体(ryanodine receptor,ryr),具有优良的胃毒作用兼一定的触杀活性,对鳞翅目昆虫有很好的防治效果,对卵和幼虫作用效果极佳,对作物药害风险小,且使用剂量低。此外,由于昆虫与其他生物间鱼尼丁受体存在差异,双酰胺类杀虫剂具有优异的选择毒性,对哺乳动物、鸟类、蜜蜂、鱼类低毒;与传统的杀虫剂无交互抗性。
以氟苯虫酰胺为首的双酰胺类杀虫剂一上市,就受到了广泛认可。随后形成了杜邦、巴斯夫、三井等公司对双酰胺杀虫剂及其制剂的开发热潮。氯虫苯甲酰胺(chlorantraniliprole)、溴氰虫酰胺(cyantraniliprole)、四氯虫酰胺(tetrachlorantraniliprole)、氟氰虫酰胺(tetraniliprole)等杀虫剂被相继开发和商品化。部分双酰胺类杀虫剂的渗透性、内吸传导性得到了提升,防治谱也从鳞翅目扩展至双翅目、鞘翅目和半翅目,不仅用于大田作物,在园艺、蔬菜种植、防治卫生害虫方面也崭露头角。氯虫苯甲酰胺和氟苯虫酰胺在2016年全球销售额分别位列杀虫剂的第1名和第8名。
然而,随着时间的推移,双酰胺的安全和抗性问题也逐渐显露。氟苯虫酰胺会在环境中分解成对一些水生无脊椎动物产生严重危害的持久性物质,2016年美国所有州开始禁用氟苯虫酰胺,使双酰胺类杀虫剂受挫严重。为了确定几个主要双酰胺类杀虫剂对有益生物的危害,开展了对家蚕、蜂类、蚯蚓、溞类、害虫天敌、羊、鱼类等的安全性评估。双酰胺类杀虫剂对鳞翅目昆虫有活性,其对家蚕的危害毋庸置疑。在浸叶法试验中,亚致死浓度的氯虫苯甲酰胺会引起家蚕变态发育;溴氰虫酰胺对意大利蜜蜂的48 h接触致死中量ld50 为3.71×10-2μg/只,属于高毒,而瓜田中推荐使用浓度的氯虫苯甲酰胺会对蜜蜂的飞行能力产生影响;对蚯蚓低毒的溴氰虫酰胺和氟苯虫酰胺被报道能够诱发蚯蚓体内的氧化胁迫,进而分别造成细胞损伤和dna损伤。
此外,我国浙江余姚、象山两地的二化螟种群中,溴氰虫酰胺、氯氟氰虫酰胺、四氯虫酰胺均与氟苯虫酰胺和氯虫苯甲酰胺存在交互抗性。
上述现状说明了双酰胺类杀虫剂在促进农业生产方面的重要性,也表明亟需开发新型双酰胺类杀虫活性物质,以解决有害生物抗性及生态安全等问题。
1 双酰胺类杀虫剂的分类
根据结构特点,双酰胺类杀虫剂主要分为邻苯二甲酰胺(phthalic diamide)和邻甲酰胺基苯甲酰胺(anthranilic diamide)两大类。这2类杀虫活性分子的经典代表分别是氟苯虫酰胺和氯虫苯甲酰胺(图1)。其他的双酰胺类杀虫剂分子,都是以二者为先导化合物,改造衍生而来的,表1列出了已登记或准备登记的双酰胺类杀虫剂有效成分。
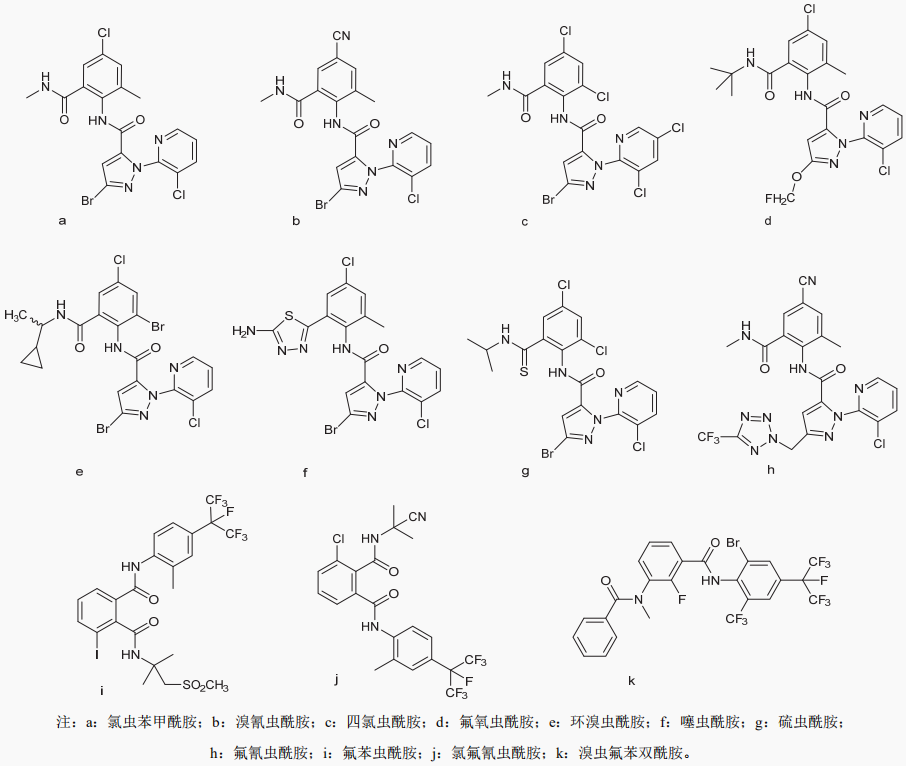
图1 已上市的双酰胺类杀虫剂的结构式
表1 目前已登记或准备登记的双酰胺类杀虫剂
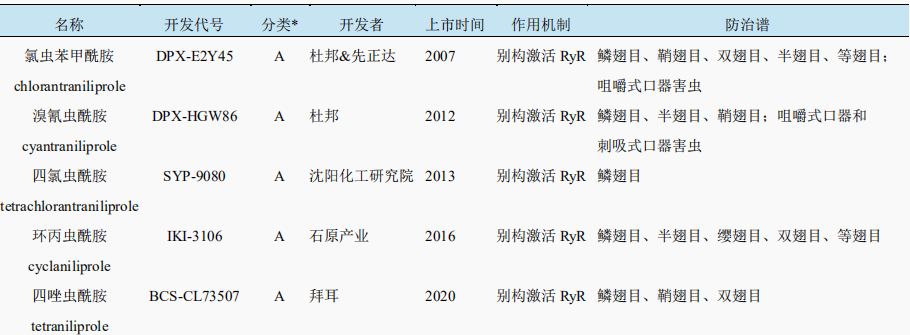
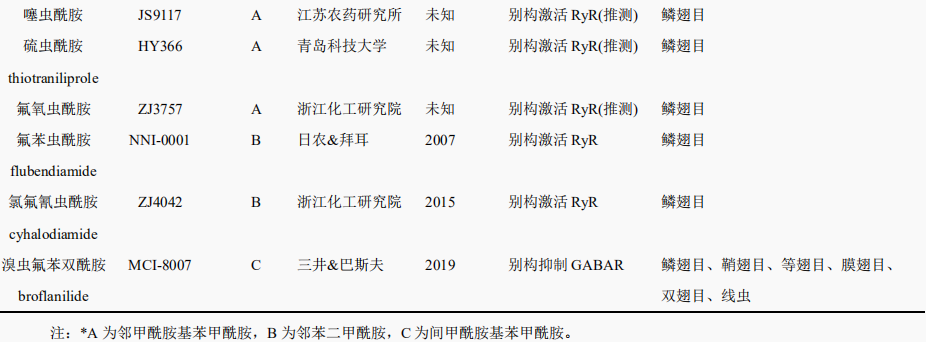
2 双酰胺类杀虫剂的作用机制
杀虫机制对于靶向设计衍生物具有重要的指导作用,下述机制介绍的主要目的是展示不同双酰胺类杀虫物质在作用位点、作用功能上的差异性,为基于构效关系(不仅仅是结构与药效,还指药物结构及其与靶标间的相互作用)的分子设计提供思路。
昆虫鱼尼丁受体ryr是位于昆虫肌肉细胞内质网(肌质网)上的ca2 门控通道蛋白之一,它含有4个相同亚基,负责控制贮存于肌质网中的大量ca2 的流出,协同肌细胞膜上的ca2 通道,调节细胞内部的ca2 水平,进而协助控制肌肉组织的收缩等重要生理活动。
目前,大多数双酰胺类杀虫分子的作用靶标是昆虫的ryr。双酰胺类ryr别构调节剂结合于ryr的特定位点,使ryr通道持续开放,一方面导致肌细胞质内ca2 水平过高,引发肌肉持续收缩;另一方面使肌质网上的ca2 泵消耗大量atp,以重新补充肌质网过度流失的ca2 ,最终虫体收缩、变短变粗,昆虫脱粪、脱水、死亡(图2)。
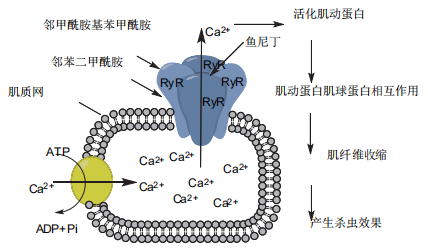
图2 双酰胺类杀虫剂的杀虫机制
从表1可以看到,大多数双酰胺类杀虫分子的作用靶标是昆虫的ryr,只有溴虫氟苯双酰胺例外。溴虫氟苯双酰胺属于间甲酰胺基苯甲酰胺,其作用靶标是γ-氨基丁酸受体(γ-aminobutyric acid receptor, gabar,也是一种cl-门控通道蛋白)。尽管与大环内酯类杀虫剂的作用区域有所重叠,但从昆虫中毒的症状来看,溴虫氟苯双酰胺对gabar的别构调节可能是抑制了其对cl-的通透性,使得细胞膜电位去极化,昆虫过度兴奋,惊厥抽搐,死亡(图 3)。
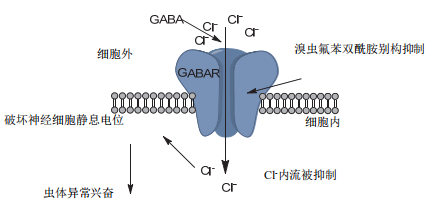
图3 溴虫氟苯双酰胺的杀虫机制
3 双酰胺类杀虫剂的合成研究
下面以氟苯虫酰胺、氯虫苯甲酰胺和溴虫氟苯双酰胺为例,介绍3类经典化合物的开发历程。
氟苯虫酰胺的研制,始于1989年大阪府立大学tsuda(津田)等对吡嗪二甲酰胺类除草剂的研究。tsuda 等报道的吡嗪二酰胺结构引起了日本农药株式会社的关注,日农公司在研发过程中,发现一种具有杀虫活性的邻苯二甲酰胺物质,能够使昆虫出现逐渐萎缩的症状。随后,日农公司先后在邻苯二甲酰胺结构的苯环上引入碘原子,提高了化合物的杀虫活性并降低了对作物的药害;将七氟异丙基置于苯胺的4-位,扩展了化合物的杀虫谱;把含硫原子的砜结构引入脂肪胺部分,大幅提高了杀虫活性。最终成功研制出氟苯虫酰胺(图1,i)。
氟苯虫酰胺的成功研制,使杜邦公司注意到邻苯二甲酰胺结构化合物的杀虫潜力,在研究过程中,研究者将苯胺和胺酰基苯之间的酰胺桥反转,得到了邻甲酰胺基苯甲酰胺分子骨架,同时将原先的苯胺替换为吡啶基吡唑,除去脂肪胺上的砜结构和苯环上的碘原子,最后引入溴原子、氯原子、甲基,得到了氯虫苯甲酰胺(图 1,a)。之后,杜邦公司将氯虫苯甲酰胺苯环上4-位的氯原子换为氰基,得到了溴氰虫酰胺(图1,b)。2008年,沈阳化工研究院又以氯虫苯甲酰胺为先导化合物,将苯环上的甲基替换为氯原子,获得了四氯虫酰胺(图1,c)。
从2002年开始,三井公司以氟苯虫酰胺为先导化合物,经10年左右开发筛选出溴虫氟苯双酰胺。在筛选过程中,首先,三井公司反转了脂肪胺酰与邻苯二甲酰之间的酰胺桥(脂肪胺酰因此变为脂肪酰胺),再将桥接的位点从邻位变为间位,形成了间甲酰胺基苯甲酰胺骨架;之后,在苯胺的邻位引入溴原子和三氟甲基,替换脂肪酰胺为苯甲酰胺等结构修饰,提高了化合物的杀虫活性;最后,用甲基替代了苯甲酰胺中氮原子上的氢原子,优化了化合物的物理性质(提高溶解性,降低生物利用度),得到了溴虫氟苯双酰胺(图1,k)。
4 双酰胺类杀虫剂的发展方向展望
在过去10年的双酰胺类杀虫剂合成研究中,丰富多样的改造、修饰工作为后来的研究者提供了大量的构效关系信息,更详尽的构效关系讨论也屡见不鲜。然而,在双酰胺化合物的设计领域,已有文献提供的信息没有被充分利用,一些设计尚缺乏针对性,主要表现在:
第一,分子对接手段可以通过模拟靶标与药物分子间的互作,为假设的化合物结构做理论初筛的参考,指导合成工作者进行双酰胺药物分子的结构设计。然而这种应用在双酰胺类杀虫剂的研发报道中尚未提及。造成这种局面的重要原因之一,可能是目前ryr蛋白质结构尚未被完全解析。
第二,近年来,双酰胺杀虫剂的抗性问题已经逐渐显现,且一些有效成分间已出现了交互抗性。这表明一些昆虫的ryr上,可能存在多个结构域的变异,更严重的情况是ryr在昆虫体内的整体表达水平可能已经下降。如果过度依赖ryr靶标杀虫剂,最终将使大部分双酰胺类杀虫剂失效,以不同ryr结构域为靶点开发新化合物也将失去意义。已商品化的溴虫氟苯双酰胺高效广谱,甚至对线虫产生了较强杀伤作用,它的靶点不同于其他双酰胺类杀虫剂,定位于gabar,而且该靶点与大环内酯类杀虫剂的gabar靶点不完全重合。如果将溴虫氟苯双酰胺和其他双酰胺类杀虫剂结合,轮替使用或合理混用,进行鳞翅目等害虫的综合治理,将会有效减缓ryr靶标失效的过程,同时起到增效减施的目的,减少药剂对环境及作物的污染。然而,以溴虫氟苯双酰胺为先导化合物进行杀虫剂开发的报道尚不多见。如果充分利用这种定位于昆虫gabar的间甲酰胺基苯甲酰胺结构,开发出一系列新型杀虫剂,将会为鳞翅目害虫的抗性综合治理提供更多选择。
第三,提升药物分子药效的手段不局限于提高其对靶标的活性。药物分子在害虫体内及其活动区域的物理行为(如溶解、吸附、扩散、内吸、植株内转运、虫体内转运)对药效的发挥有着不容小觑的影响,通过合理的结构设计,使化合物的物理特性更有利于其接近作用靶标,也是一种提高药效的办法。由于目前双酰胺类杀虫剂的探索历史只有短短十几年,药物分子物理行为的研究在双酰胺杀虫剂中尚不多见。xu 团队关于“甘氨酸-氯虫苯甲酰胺”偶联分子的工作,提供了双酰胺药物在植株内转运机制的研究参考;兰州大学张娜提出的“硅原子可能提升药物分子亲脂性”的想法也有待验证。双酰胺类杀虫剂的物理行为仍有很大探索空间。
综上,双酰胺杀虫剂今后的研究将集中于“ryr 晶体结构解析”“邻甲酰胺基苯甲酰胺与ryr 靶标的构效关系”“以溴虫氟苯双酰胺为先导的药物开发”“促进双酰胺杀虫剂分子从施放到接触靶标的有效物理迁移”“害虫对双酰胺化合物抗性的综合治理”等领域。

(1)本网旨在传播信息,促进交流,多方面了解农药发展动态,但不构成任何投资建议。
(2)所有文章仅代表作者观点,不代表本网立场。
(3)“信息来源:江苏省农药协会 农药资讯网”为原创文章,转载时请注明来源和作者。
(4)本网转载文章及图片的凯发k8国际的版权属于原作者,若有侵权,请联系删除。